El síndrome de congestión pélvica (SCP) o varices pélvicas (VP) es una entidad que pueden sufrir millones de mujeres en el mundo, y su ocurrencia puede llegar hasta un 39%. Son múltiples los factores que contribuyen la patofisiología del SCP. Hasta un 15% de las mujeres entre las edades de 20 a 50 años tienen venas varicosas en la pelvis, aunque no todas experimentan síntomas.
ObjetivoDeterminar la eficacia y seguridad de la flebografía y embolización de las VP como noxa del SCP.
Material y métodosSe incluyeron, desde junio de 2014 hasta diciembre de 2015, 75 mujeres sintomáticas remitidas de otros centros con diagnóstico de SCP; de ellas 24 pacientes (edades comprendidas entre 26 a 55 años con una media de 37 años) reportaron presencia de VP confirmadas con ultrasonido transvaginal (UST), posteriormente a este grupo se le realizó una flebografía control para ratificar dicho diagnóstico e inmediata embolización si así lo requerían. Se estableció el score escala analógica visual para determinar clínicamente el éxito del procedimiento con seguimiento a los 3, 6, 9 y 12 meses, correlacionando con el de base previo al procedimiento; además se realiza UST a los 6 meses para determinar el cierre o recanalización, y una flebografía control a los 12 meses con el mismo objetivo. Estos parámetros se recogieron en una plantilla base.
ResultadosLa presencia de VP asociada a SCP en nuestra ciudad, por ser nuestra institución centro de referencia nacional, constituyó un 3,9% de la población femenina recibida durante el año 2015. El 100% (n=24) de nuestras pacientes fue sintomática, donde la dispareunia era uno de los factores mayormente referido (100%); además el 100% de la población estudiada presentó como factor de riesgo la multiparidad y solo un 37% de ellas mostró varices en los miembros inferiores; cuando se realizó la flebografía control solamente en el 83% (n=20) de las pacientes referidas por US transvaginal con VP se confirmó el diagnóstico. Posteriormente al procedimiento no tuvimos complicaciones, el 8,3% de pacientes presentó recurrencia de síntomas a los 9 meses de seguimiento, se les realizó una flebografía control y se embolizó los vasos venosos ectásicos dependientes de la vena iliaca interna derecha y gonadal derecha, respectivamente. Al seguimiento a los 12 meses no tuvimos recurrencia de síntomas en ninguna de ellas. No tuvimos diferencias en el éxito de oclusión con el uso de coils vs polidocanol.
ConclusiónLa flebografía es un método específico y con baja tasa de complicaciones para el diagnóstico de VP. La embolización de VP con uso de coils o polidocanol representa un método eficaz y seguro como tratamiento del SCP.
Pelvic congestion syndrome (PCS), or pelvic varices (PV), is an entity suffered by millions of women worldwide, and its occurrence can reach up to 39%. Multiple factors contribute the pathophysiology of the PCS. Up to 15% of women between the ages of 20 and 50 years-old have varicose veins in the pelvis, although not all experience symptoms.
The aim of this study was to determine the efficacy and safety of phlebography and embolisation of the PV as treatment for PCS.
Material and methodsThe study included 75 symptomatic women, who were enrolled from June 2014 to December 2015 after being referred from other centres with a diagnosis of PCS. Of these, 24 patients (aged 26-55 years with a mean of 37 years) were diagnosed with the presence of PV using transvaginal ultrasound. A venography was performed on this group to verify the diagnosis, and immediate embolisation was performed, if this was possible and required. The VAS score was measured to clinically determine the success of the procedure at 3, 6, 9, and 12 months of follow-up, correlating with prior to the procedure base. Transvaginal ultrasound was also performed at 6 months to determine the closure or rechannelling, as well as a phlebography at 12 months, with the same objective. These parameters were collected in a base template.
ResultsThe presence of PV associated with PCS in our city, due to being a central institution of national reference, was 3.9% of the female population seen from June of 2014 to December 2015. All the 24 patients were symptomatic, with dyspareunia being one of the most referred to factors; 100%. All the study population presented with multiparity as risk factor, and only 37% of them showed varices in the lower limbs. When phlebography was performed the diagnosis was confirmed in only 83% (n=20) of patients referred due to PV observed in the transvaginal ultrasound. There were no complications during the follow-up of the procedure, 8.3% of patients had recurrence of symptoms at 9 months follow-up. A phlebography was performed and ectatic venous vessels dependent on the right internal iliac vein and gonadal right were embolised, respectively.
There was no recurrence of symptoms in any of them after 12 months of follow-up. No differences were observed in the successful occlusion with the use of coils vs polidocanol.
ConclusionPhlebography is a specific test and with a low complication rate for the diagnosis of PV. Embolisation of pelvic varices using coils or polidocanol is an effective and safe method for the treatment of PCS.
El dolor pélvico crónico (DPC) en la mujer es frecuente en edades reproductivas; afecta generalmente en el período de los 20 a los 50 años de edad, y su frecuencia va desde un 15% a un 39% de la población femenina1–3.
El síndrome de congestión pélvica (SCP) es una causa importante de dolor pélvico visceral de origen ginecológico asociado a varices pélvicas, y se caracteriza por dolor pélvico pertinaz e incapacitante, y en donde no es fácil determinar la causa patológica de su origen si no existe la sospecha diagnóstica previa por el médico tratante, basado en una historia clínica sugestiva de dicha condición3–5.
Por muchos años, y basado en los estudios de Duncan y Taylor, a finales de la década de los 40 se consideró el SCP mediado por varices como una enfermedad psicosomática por su asociación con depresión, cefalea e insomnio5–8. Esta desafortunada tendencia se originó en un estudio clínico no aleatorizado, con una muestra muy pequeña de pacientes, sin contar con los recursos actuales de diagnóstico como flebografía, UST o resonancia magnética nuclear6–8.
El síndrome solo empezó a ser reconocido como un dolor de origen visceral por los trabajos de Beard et al. en la década de los 80, quienes encontraron que el 91% de las mujeres con DPC sin una causa objetiva en la laparoscopia presentaban varices pélvicas al realizar flebografía pélvica, y tuvieron una mejoría notable de sus síntomas al realizárseles histerectomía más salpingooforectomía bilateral8–12.
La embolización es una técnica que ha demostrado seguridad y eficacia para el tratamiento del SCP en pacientes con hipertensión venosa pélvica (HVP) desde hace mas de 15 años13–17. Se realizó este estudio para determinar la presencia de VP y su asociación con la clínica, así como determinar el diagnóstico y la respuesta al tratamiento de embolización durante el seguimiento a un año.
ObjetivosDemostrar el éxito del procedimiento de embolización a través del seguimiento con la evaluación sintomática y diagnóstica por imagen de las varices pélvicas como noxa del dolor pélvico crónico, además de establecer la presencia de alguna complicación trans o postintervención de las pacientes que acudieron a nuestra consulta durante el mes de enero de 2015 hasta diciembre de 2015.
Hipótesis- 1.
La flebografía es un método específico y sensible de diagnóstico de varices pélvicas, pero también tiene su objetivo terapéutico inmediato.
- 2.
El tratamiento endovascular es una opción terapéutica, segura por la baja tasa de complicaciones y eficaz, con alto éxito clínico inmediato y a largo plazo. La mejoría o la remisión de los síntomas es inmediata al mes de tratamiento y a largo plazo.
- 3.
El uso de agentes embolizantes líquidos vs coils no posee diferencias significativas en cuanto a la aparición de síntomas recurrentes o de recanalización postembolización, tienen el mismo éxito de oclusión inmediato.
Se realizó un estudio cuasi experimental de pacientes enviadas a nuestro servicio para tratamiento de SCP asociado a HVP, confirmadas por UST desde junio de 2014 hasta diciembre de 2015.
Se realizó una flebografía a todas las mujeres de forma consecutiva que cumplían los criterios clínicos y de imagen por US doppler pélvico y transvaginal de SCP.
Se realizó una entrevista y examen físico previamente para recolectar los datos clínicos y resultados previo al estudio angiográfico, y posteriormente se controló en consulta a los 3 meses, 6 meses, 9 meses y al año.
El nivel de dolor fue categorizado previo y posterior a la embolización y durante el seguimiento usando la escala análoga visual (VAS) y plasmando en una plantilla base.
Al año posprocedimiento se realizó una flebografía control y a los 6 meses un UST que permite determinar la oclusión de las gonadales y/o vasos intervenidas.
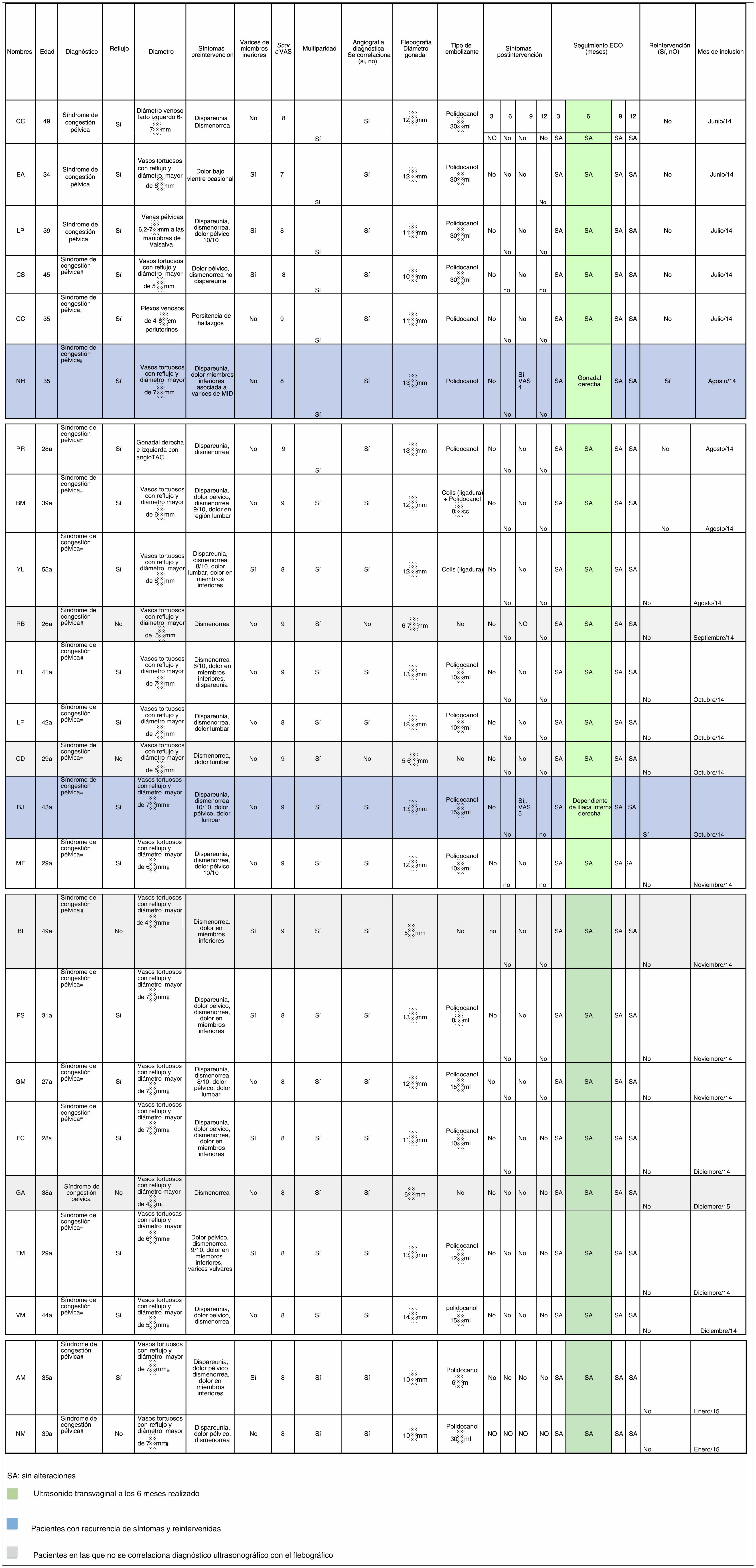
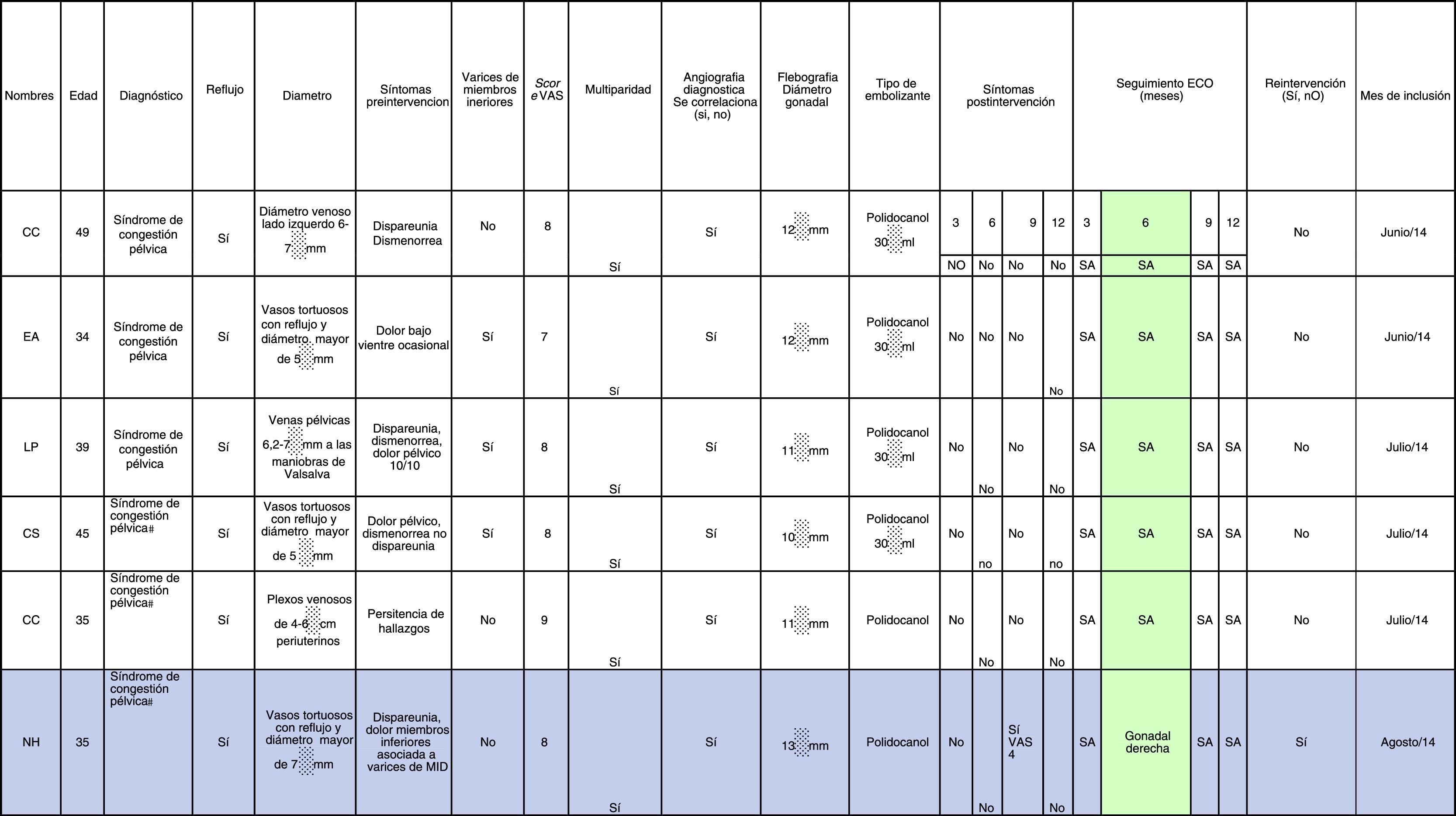
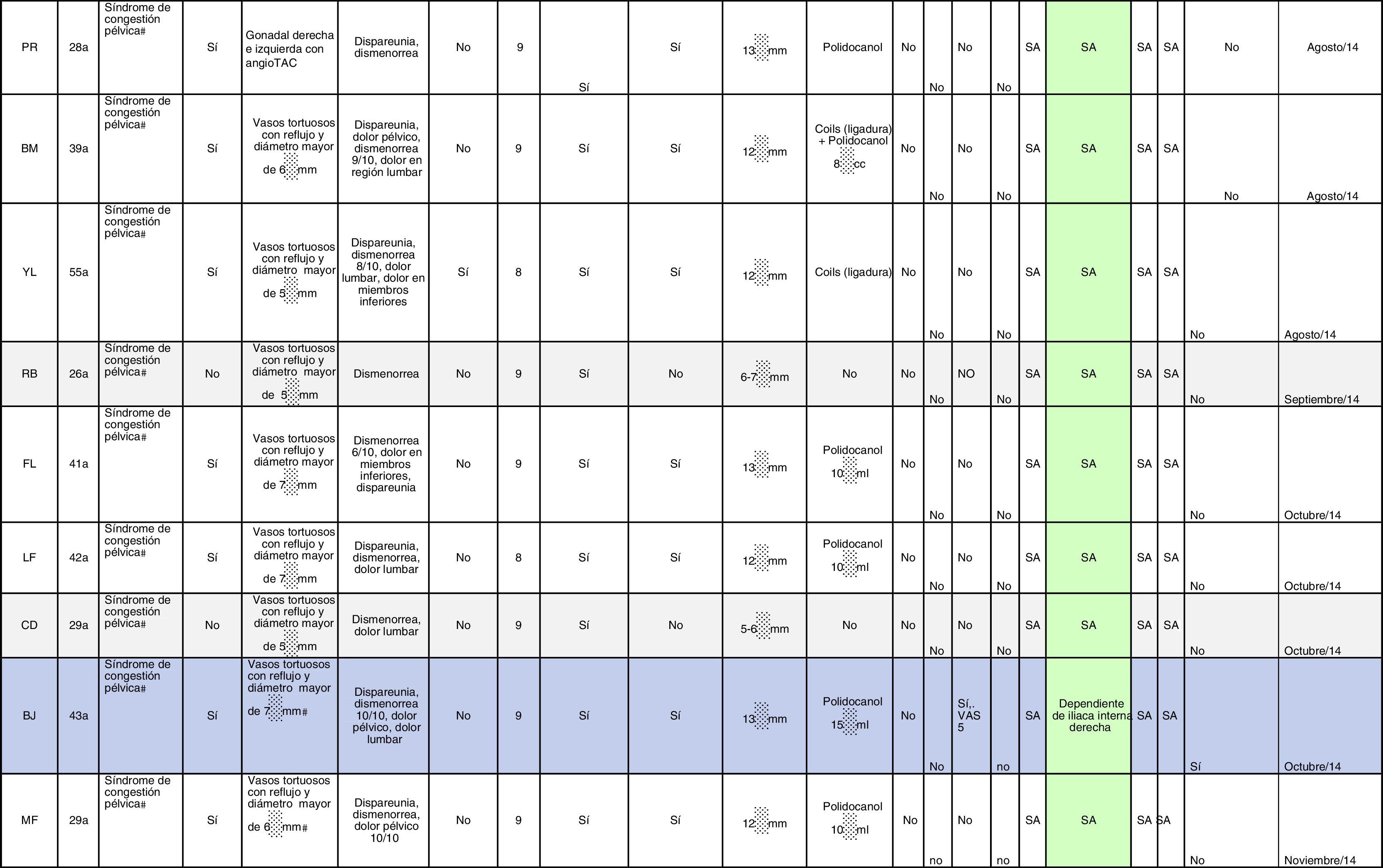
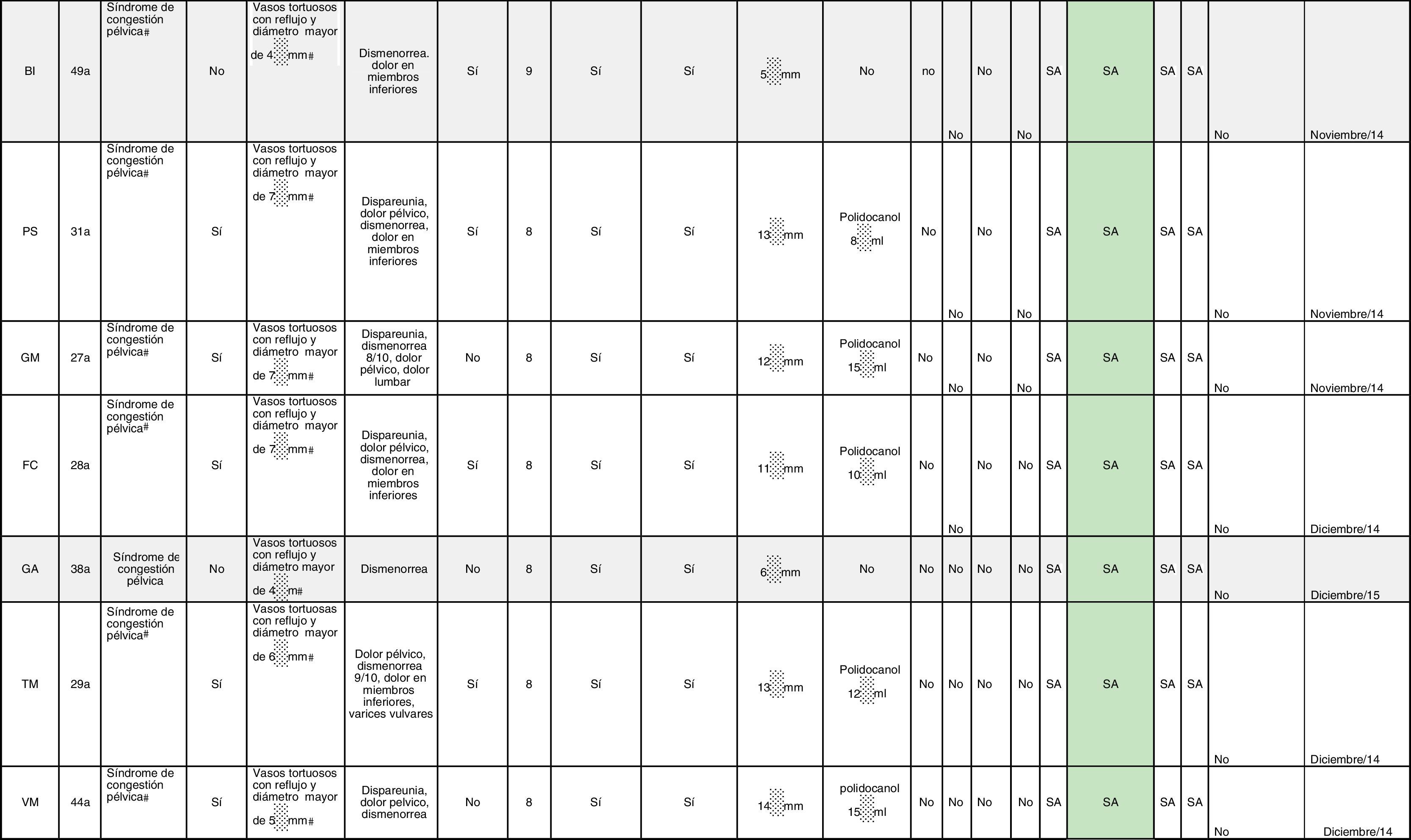
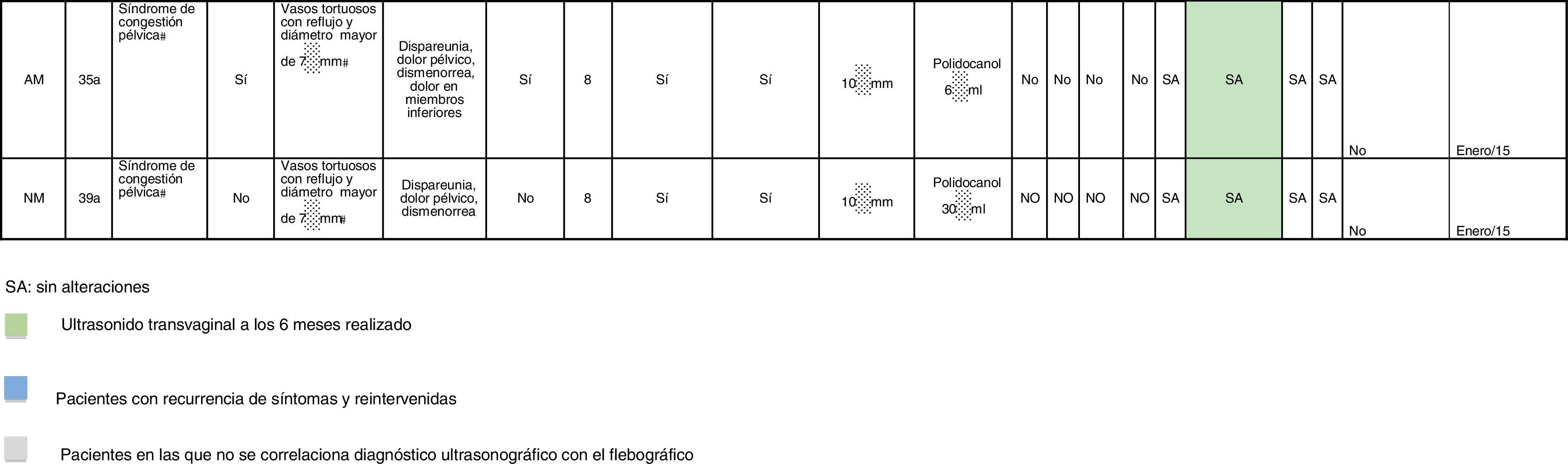
Todos estos datos fueron llevados a una plantilla que recogió todos los datos mencionados (tabla 1).
ResultadosNuestro servicio tomó un grupo de pacientes que fueron incluidas desde junio de 2014 hasta diciembre de 2015 de forma consecutiva; 79 mujeres fueron diagnosticadas de SCP y recibidas en el Servicio de Cirugía Vascular, Angiología y Endovascular del Hospital Enrique Garcés. Veinticuatro de ellas presentaron el diagnóstico de SCP por ultrasonido pélvico y transvaginal, las cuales fueron nuestra población objetivo, y se les sometió a una flebografía control, con lo cual se obtuvieron los resultados que se muestran en la tabla 2.
Resultados
| Pacientes Número (porcentaje) N=24 | Resultados |
|---|---|
| 20 (83) | Pacientes en las que se correlacionaba su sintomatología de SCP con la presencia de varices pélvicas por flebografía (criterios) |
| 8 (33) | Pacientes que presentaron como factor de riesgo la presencia de varices en los miembros inferiores |
| 24 (100) | Pacientes que presentaron factores de riesgo como multiparidad (definida como más de un hijo) |
| 24 (100) | Pacientes que no tuvieron complicaciones relacionadas con el procedimiento diagnóstico y/o terapéutico |
| 18 (90) | Pacientes que presentaron desaparición de sus síntomas durante el seguimiento |
| 2 (10) | Pacientes que presentaron dolor recurrente a los 9 meses |
| 2 (10) | Pacientes que recibieron coils y polidocanol |
| 0 (0) | Pacientes con solo coils |
| 18 (90) | Pacientes con solo polidocanol |
Según escala VAS de dolor preembolización este fue significativamente menor después de la embolización, como queda demostrado en la tabla 3.
DiscusiónMillones de mujeres en el mundo pueden sufrir de DPC en algún momento de su vida, llegando hasta un 39,1%. El DPC representa del 10% al 15% de las pacientes recibidas en la consulta de ginecología en Estados Unidos. El SCP fue descrito inicialmente por científicos Gooch en 1821, pero documentado solo fue hasta 1949, fecha en la que Taylor propuso la relación entre el DPC y las varices pélvicas1–5.
No se conocen con claridad sus características genéticas, etiológicas o fisiopatológicas, pero se ha establecido una fuerte relación entre el diagnóstico y las pacientes en edades reproductivas, especialmente aquellas multíparas con edades entre 20-45 años de edad1–14,18,19. En nuestro estudio se evidenció que el 100% de las pacientes se encontraban en etapa reproductiva y el 100% eran multíparas, en correlación con la bibliografía mundial.
Las mujeres con múltiples embarazos tienen una predisposición mayor para el SCP por el hecho de que el volumen intravascular durante el embarazo aumenta considerablemente, y la capacidad venosa se puede incrementar hasta en un 60%; esto conlleva que, con el tiempo, la distensión venosa pueda crear una incompetencia valvular al nivel de las venas pélvicas2–6. Adicionalmente, el aumento de peso y las alteraciones pélvicas anatómicas que van de la mano con el embarazo pueden producir compresiones venosas intermitentes a este nivel7–19.
Es muy complejo enmarcar las diferentes variables clínicas y diagnósticas de las varices pélvicas y su asociación con el SCP, por lo que existe confusión acerca de la entidad en estudio; sin embargo, la literatura agrupa 4 diferentes grupos de acuerdo a los hallazgos diagnósticos encontrados y la presencia o ausencia de dolor pélvico sugestivo de congestión pélvica20:
Grupo 1: pacientes con síntomas de dolor pélvico sugestivo de congestión pélvica, incluyendo vasos venosos pélvicos dilatados con aclaramiento reducido al medio de contraste, pero no necesariamente reflujo ovárico venoso anterógrado.
Grupo 2: pacientes con varices vulvares y reflujo venoso ovárico, con o sin dolor pélvico sugestivo de congestión pélvica.
Grupo 3: pacientes con dolor pélvico sugestivo de congestión pélvica y dilatación de venas ováricas u otras venas pélvicas vistas en estudios de resonancia magnética o ultrasonido doppler.
Grupo 4: pacientes que están asintomáticas pero tienen varices pélvicas o reflujo de vena ovárica a la flebografía u otros estudios diagnósticos.
De acuerdo con esta clasificación solo una paciente (n=1) de las 20 embolizadas presentó varices vulvares, que ameritó 3 sesiones de embolización directa además de la embolización gonadal izquierda, correspondiente al grupo 2; el resto de pacientes (n=19) fueron del grupo 3.
En cuanto a la clínica la dispareunia es común, además se presenta ocasionalmente como un signo muy característico el dolor poscoital, que puede durar horas o días llevando secundariamente a disfunción sexual15–17,21,22,24–30, como refieren el 100% de nuestras pacientes.
Para la confirmación del diagnóstico de síndrome de congestión pélvica se requiere observar las venas de la pelvis engrosadas (más de 5mm) con flujo pobre en su interior, por lo cual se requieren pruebas imagenológicas dinámicas, siendo la flebografía la prueba de oro para el diagnóstico del SCP, con el gran inconveniente de que es un examen invasivo. La flebografía puede ser transuterina o transfemoral selectiva20,31. La flebografía transuterina puede realizarse de manera ambulatoria.
Los hallazgos a la flebografía que sugieren congestión pélvica son: diámetro de la vena ovárica de 10mm en su punto más ancho, ingurgitación venosa uterina, congestión moderada o intensa del plexo ovárico, llenado de venas cruzando la línea media o llenado de las varicosidades vulvares o del muslo. La presencia de más de uno de los factores anteriores se considera como prueba importante de apoyo en el diagnóstico32.
La flebografía selectiva ovárica se realiza por vía percutánea a través de la vena femoral o la vena yugular interna y posterior cateterización selectiva de la vena ovárica izquierda con la paciente en posición semierguida; después, el procedimiento se repite para el lado derecho o si es necesario se realiza cateterización de venas hipogástricas. Este tipo de intervención puede o no requerir hospitalización por un día, pero provee mayor y mejor información que la vía transuterina y es mejor tolerada por la paciente, además también permite la subsecuente embolización en los centros donde se realiza este manejo33,34.
En la mayoría de los casos las varices pélvicas y el SCP no son diagnosticadas con los métodos convencionales de exámenes ginecológicos como el ultrasonido abdominal o transvaginal32.
Hobbs, en su revisión de 199035, encontró que un número importante de varices visibles a la flebografía no eran diagnosticadas por ultrasonido; Park et al.36, usando ultrasonido doppler, encontraron un grado de consistencia razonable entre los hallazgos de flebografía y aquellos usando ultrasonido vaginal doppler. Sin embargo, se reporta un 17% de falsos positivos y adicionalmente en el 90% de las pacientes no es posible visualizar la arteria ovárica derecha23,24,26,28,29,33,34,25,37.
En nuestro estudio se determinó que de 24 pacientes con SCP y USG transvaginal que refería la presencia de VP, solo en el 83% se confirmó el diagnóstico, como lo refiere la bibliografía en cuanto la baja sensibilidad de la USG transvaginal o abdominal.
Esto representa una tasa de incidencia en nuestra población de Quito de 3,4% de mujeres que padecen de SCP asociado a la presencia VP, correspondiente este valor con lo referido en la bibliografía.
En cuanto al tratamiento, desde que Topolansk Sierra38 y su grupo de trabajo establecieron por primera vez la relación entre el DPC y las varices pélvicas en las década de 1950 se han propuesto muchas modalidades de tratamiento.
A nivel quirúrgico, inicialmente se intentó tratar a las pacientes por medio de histerectomía o ventrosuspensión del útero en retroversión, como iniciativa para aliviar la sintomatología; sin embargo, estudios posteriores lograron evidenciar que tales procedimientos no iban a traducirse en mayor mejoría clínica para las pacientes, ya que se encontraron tasas de dolor residual de hasta un 33% y recurrencias de un 20% aproximadamente, debido a que la etiología del SCP venía de la mano con una incompetencia de las venas ováricas. En la década de los 80 Rundqvist et al.39 plantearon la resección extraperitoneal de la vena ovárica izquierda. Dicho procedimiento demostró disminuir considerablemente los síntomas del SCP, así comola ligadura laparoscópica, pero con mayor tiempo de hospitalización y anatesia general23,40,41.
En 1993 se introduce la embolización endovenosa pélvica por Edwards et al.42, lo cual se convirtió en un método revolucionario. La embolización pélvica es un procedimiento que asocia leve dolor postoperatorio con una rápida recuperación, de ahí que se considere en muchos centros un procedimiento ambulatorio con tasas de éxito técnico que alcanzan el 99% y baja tasa de complicaciones, por debajo del 5%20,28,29,40,41,43,44.
Nuestro estudio demostró una tasa de éxito del 100% inmediato; a pesar de las recurrencias que tuvimos cabe aclarar que eran pacientes que presentaban varices asociadas a vasos poco frecuentes, como la iliaca interna derecha o gonadal derecha, y que no fueron embolizados en un primer término; a pesar de ello el éxito clínico fue inmediato y sin complicaciones, como lo demuestra la bibliografía. Además, usando la escala VAS39, donde evaluamos la remisión o recurrencia de síntomas pre y postembolización, obtuvimos valores significativamente menores con una media de dolor de 8,2 puntos preprocedimiento y postembolización; a los 3 y 6 meses fue de 0 puntos, en el mes 9 tuvimos 2 pacientes con recurrencia de síntomas que corresponde al 10% de las pacientes sometidas a embolización, pero posterior a la nueva embolización actualmente no presentan remisión de síntomas28–30,40,41,43,44.
ConclusionesEl SCP constituye un problema de salud pública, es una enfermedad frecuente, muchas veces subdiagnosticada, generando altos costes para los servicios de salud. Pese a que los métodos diagnósticos son variados, aún están poco difundidos, siendo el SCP una causa frecuente de dolor pélvico sin diagnóstico.
La flebografía representa un excelente modelo diagnóstico altamente efectivo por la correlación entre la clínica de SCP y la presencia de VP, además ofrece terapéutica inmediata. La oclusión de las venas ováricas inmediata al estudio angiográfico en el SCP es un procedimiento factible y seguro por los resultados alentadores a corto y largo plazo, tiene la ventaja de ser ambulatoria, se realiza con anestesia local, permite una reinserción laboral inmediata y presenta baja tasa de complicaciones.
Se requiere trabajo multidisciplinario (clínicos generales, ginecólogos, flebólogos y endocrinólogos y endovasculares) para obtener mejores resultados. En la mayoría de pacientes el tratamiento endovascular ofrece una alternativa eficaz con mejores beneficios clínicos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.