Debido a las características electromagnéticas únicas del microhilo amorfo magnetoelástico, los cambios en la presión de un fluido provocarán una variación de la tensión mecánica sobre el sensor, lo que supondrá una variación de su imanación que será detectable de forma inalámbrica. Utilizando esta tecnología, se podrá desarrollar un sistema inalámbrico para el seguimiento de procedimientos en cirugía vascular.
MétodosEl sensor diseñado consiste en un anillo de microhilo magnetoelástico que se integró en un modelo in vitro con flujo pulsátil. Se simularon distintos grados de estenosis en distintas localizaciones, tanto en arteria bovina como en un segmento de PTFE. Se realizó el análisis de Fourier de las señales registradas, y se emplearon el test de correlación de Pearson y curvas COR para el análisis de la información.
ResultadosSe obtuvo un índice de correlación de Pearson de 0,945 (p<0,001) entre la presión invasiva del fluido y la potencia de la señal emitida por el microhilo magnetoelástico en arteria bovina. Se obtuvieron unas excelentes curvas COR, tanto en el caso de las estenosis preanastomóticas (AUC 0,98; IC 95%: 0,97-1) y anastomóticas (AUC 0,93; IC 95%: 0,86-0,99), como en el caso de las estenosis distales (AUC 0,88; IC 95%: 0,79-0,98), comparadas con un grupo control.
ConclusionesEl microhilo magnetoelástico es capaz de detectar, localizar y cuantificar el grado de estenosis en arteria bovina, así como en una anastomosis latero-terminal, con una elevada potencia estadística. Por primera vez se ha desarrollado un sensor inalámbrico in vitro para el seguimiento postoperatorio de los procedimientos en cirugía vascular.
Due to the unique electromagnetic characteristics of the magnetoelastic microwire, the changes in the pressure of a fluid will lead to changes in the mechanical pressure on the sensor, which will then cause a variation of its magnetisation which will be detectable wirelessly. Thus, a wireless system can be developed for following-up vascular surgery procedures.
MethodsThe sensor consists of a magnetoelastic microwire ring which was integrated into an in vitro model with pulsatile flow. Different degrees of stenosis were simulated in different locations in bovine artery, as well as in a polytetrafluoroethylene anastomosis. A Fourier analysis of the registered signals was performed, with a statistical analysis using Pearson test and ROC curves.
ResultsA Pearson index of .945 (P<.001) was obtained between the invasive pressure of the fluid and the power of the signal transmitted by the sensor in bovine artery. The sensor obtained very good ROC curves in the analysis of the registered the signals, in the case of pre-anastomotic stenosis (AUC .98; 95% CI: .97-1), anastomosis (AUC .93; 95% CI: .86-.99), as well as distal (AUC .88; 95% CI: .79-.98), compared to the control group.
ConclusionsThe magnetoelastic microwire has shown that it is capable of detecting, locating and quantifying the degree of stenosis in bovine artery, as well as in a latero- terminal anastomosis, with a high statistical power. For the first time, a wireless in vitro sensor has been developed for the post-operative follow-up of vascular surgery procedures.
La enfermedad arterial periférica (EAP) es el conjunto de signos y síntomas que se producen como consecuencia de la disminución progresiva del flujo sanguíneo en las extremidades inferiores.
Se estima que la prevalencia de esta enfermedad se encuentra entre el 3 y el 18%, lo que supone más de 27 millones de personas afectadas en todo el mundo1-4.
Aproximadamente entre un 50-90% de los pacientes con isquemia crítica se someterán a un procedimiento de revascularización mediante cirugía convencional o técnicas endovasculares5.
El fracaso de los procedimientos quirúrgicos, tanto abiertos como endovasculares, continúa siendo un desafío y está asociado a una elevada tasa de morbimortalidad, por lo que el seguimiento exhaustivo es clave para mantener la permeabilidad a largo plazo de estos procedimientos.
Actualmente, los programas de seguimiento consisten en un examen físico minucioso, en la realización de pruebas no invasivas (índice tobillo-brazo, curvas de presión-volumen, fotopletismografía y eco-Doppler), y finalmente en la realización de pruebas como el angio-TC o la arteriografía en el caso de sospecha de un fracaso hemodinámico.
Dada la edad avanzada, la elevada morbilidad y la movilidad reducida de muchos de los pacientes con isquemia crítica de las extremidades, la optimización de dichos protocolos, así como la atención ambulatoria de estos pacientes, es fundamental para mantener su calidad de vida. A pesar de la importancia del seguimiento de la cirugía de revascularización arterial, existe una falta de consenso en la literatura en cuanto a su eficacia, en la forma en la que debe llevarse a cabo, así como en su duración.
La creciente carga asistencial y económica producida por el envejecimiento de la población y el aumento de la incidencia de las enfermedades crónicas constituyen un poderoso incentivo para desarrollar nuevas estrategias para el cuidado de estos pacientes, produciéndose un aumento del interés en la última década en la investigación de sistemas portátiles de medición de distintos parámetros fisiológicos.
El desarrollo tecnológico ha dado lugar al creciente interés en la investigación de nuevos biosensores cuyo objetivo es simplificar los métodos diagnósticos actuales y por lo tanto mejorar la asistencia médica, ya que mejora la calidad de vida de los pacientes y permite la atención ambulatoria de numerosas enfermedades, evitando hospitalizaciones innecesarias.
Los sensores magnéticos se encuentran a la cabeza del desarrollo tecnológico experimentado en este campo en las últimas décadas, ofreciendo numerosas ventajas debido a su elevada sensibilidad, pequeño tamaño, sistemas sin necesidad de una fuente externa de energía y conexiones inalámbricas. La utilización de tecnologías wireless sensors networks (WSN) ofrece la posibilidad de desarrollar sensores biomédicos implantables que permitan realizar la monitorización y seguimiento de ciertos parámetros fisiológicos con medidas precisas y hasta ahora impensables.
Los principales objetivos de la presente investigación son:
- 1)
Demostrar la aplicabilidad del microhilo como elemento sensor inalámbrico de variaciones de presión.
- 2)
Demostrar la aplicabilidad del microhilo como elemento sensor inalámbrico en el diagnóstico de estenosis arteriales y en una anastomosis de politetrafluoroetileno (PTFE).
- 3)
Desarrollar un dispositivo inalámbrico para el seguimiento de procedimientos en cirugía vascular mediante telemetría.
Un microhilo magnético (MH) es un filamento con estructura amorfa cuyo núcleo se compone de una aleación de metales —los más frecuentes son el hierro y el cobalto— recubierto de pyrex, que es un aislante fabricado mediante una técnica de enfriamiento ultrarrápido que permite obtener microhilos con un diámetro máximo de 100 micras.
El MH reúne 2 características únicas que le convierten en un excelente elemento sensor. Por un lado, su elevada magnetostricción junto a su baja anisotropía hacen que sea extremadamente sensible a pequeños cambios en la tensión mecánica y que esos cambios se traduzcan en cambios en su imanación al ser sometido a un campo magnético externo.
Además, debido a su elevada susceptibilidad magnética junto a su diámetro del orden de micras, es capaz de modular una señal de alta frecuencia emitida por una antena. De esta forma, los cambios en la presión de un fluido provocarán una variación de la tensión mecánica sobre el sensor, lo que supondrá una variación de su imanación y de la onda emitida que será detectable de forma inalámbrica a través de una antena receptora6-9. Por ello, es posible utilizar un anillo de este material como elemento sensor inalámbrico de presión.
El sensor diseñado consiste en un anillo de microhilo bobinando, 30cm de microhilo magnetoelástico (referencia de la patente ES2524733).
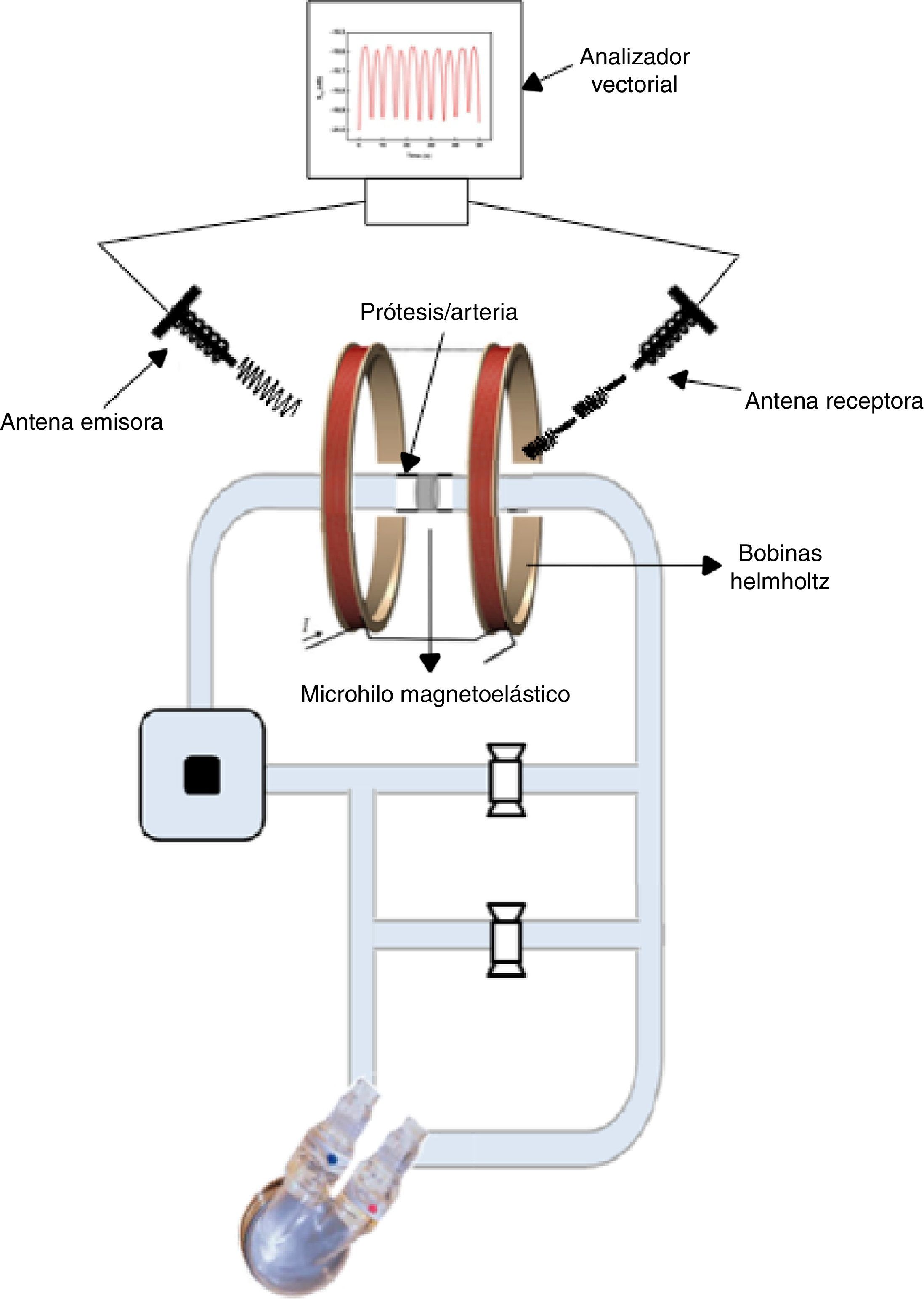
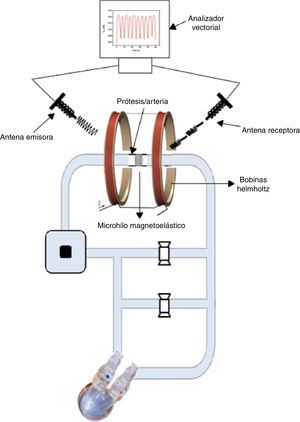
Montaje experimentalCircuito electromagnéticoEl conjunto sensor-arteria/prótesis es sometido simultáneamente a un campo magnético periódico de baja frecuencia (0,1Hz) (campo magnético BIAS) generado por unas bobinas Helmholtz y a una onda electromagnética de alta frecuencia (1,29GHz) procedente de una antena emisora. El BIAS permite la modulación de la onda emitida por el microhilo a través de su imanación y desimanación. Las variaciones de tensión mecánica sobre el elemento sensor supondrán una variación de la onda emitida detectable mediante una segunda antena receptora. Ambas antenas son de tipo helicoidal y están conectadas a un analizador vectorial de forma que obtendremos una variación de potencia debido a las distintas presiones.
Modelo de flujo pulsátilDicho modelo (arteria/prótesis sensorizada) se incluyó en un circuito con flujo pulsátil conectado a un sistema de asistencia ventricular (Abiomed/AB5000®), y a un sello de agua junto con 2 resistencias en paralelo que nos permitieron controlar la presión del fluido en todo momento al poder modificar la resistencia global del circuito.
El fluido es una disolución al 0,33% de agar-agar para obtener un coeficiente de viscosidad similar al de la sangre a 37°C (0,04poise). La arteria utilizada es un segmento de 5-10cm de arteria renal bovina conservada en suero salino fisiológico durante un periodo inferior a 48h. La prótesis utilizada es PTFE de 6mm (Maxiflo®, Vascutek®, Escocia, Reino Unido).
Para poder registrar en cada instante la presión real del fluido que atraviesa la arteria o la prótesis, se conectaron 2 sistemas de medición invasiva de presión tanto distal como proximalmente al elemento sensor. El índice de presión es el cociente entre ambos valores. En la figura 1 se puede observar la integración de ambos modelos.
Mediciones realizadasLa investigación se dividió en 3 apartados con objetivos claramente diferenciados. Cada registro de la onda emitida por el dispositivo tuvo una duración de 2s.
- 1.
Cuantificar la presión del fluido en prótesis y arteria bovina: se realizaron 128 mediciones en PTFE y 96 en arteria bovina para cuantificar la presión del fluido mediante el dispositivo inalámbrico y comparar la señal registrada con la presión real del fluido detectada mediante el sistema de medición invasivo.
- 2.
Localización y grado de estenosis en prótesis y arteria bovina: se realizaron 32 registros sin estenosis que fueron utilizados como grupo control. Posteriormente, se simularon 128 estenosis mediante una pinza que fueron divididas en 4 grupos en función del índice de presión y de su localización, pudiendo situarse en posición previa al elemento sensor o posterior al mismo.
- 3.
Localización y grado de estenosis en una anastomosis latero-terminal con PTFE: el microhilo se implantó proximal a la anastomosis (grupo A) o distal a la misma (grupo B). Se realizaron 32 registros sin estenosis que fueron utilizados como grupo control. Posteriormente, se realizaron 96 registros en cada grupo, simulando estenosis del injerto, de la anastomosis y distal a la misma mediante una pinza.
Para el análisis de la información obtenida se utilizó el programa informático Wolfram Alpha Mathematica®, realizando las transformadas de Fourier (FA) de las ondas obtenidas con el microhilo.
En nuestro caso hemos trabajado con la potencia de la FA, escogiendo las potencias tanto de la frecuencia BIAS (establecida en 0,1Hz), como de la frecuencia (en torno a 0,7Hz) en la que se transmitía la onda emitida debido al flujo pulsátil obtenido, denominada señal MH.
Análisis estadísticoSe empleó el test de correlación de Pearson para estudiar la asociación entre las variables independientes y las variables de respuesta cuantitativas. Se calcularon curvas COR para determinar los puntos de máxima sensibilidad y especificidad en las variables cuantitativas dependientes que predecían la presencia de estenosis en el modelo experimental. Para todas las pruebas se aceptó un valor de significación del 5%. El procesamiento y análisis de datos se realizaron mediante el paquete estadístico SPSS 22.0.
ResultadosCuantificar la presión del fluido en prótesis y arteria bovinaMedición de la presión del fluido en prótesis de PTFELa presión mínima registrada fue de 45mmHg y la máxima de 205mmHg, con una presión media de 120mmHg (DE 27,3).
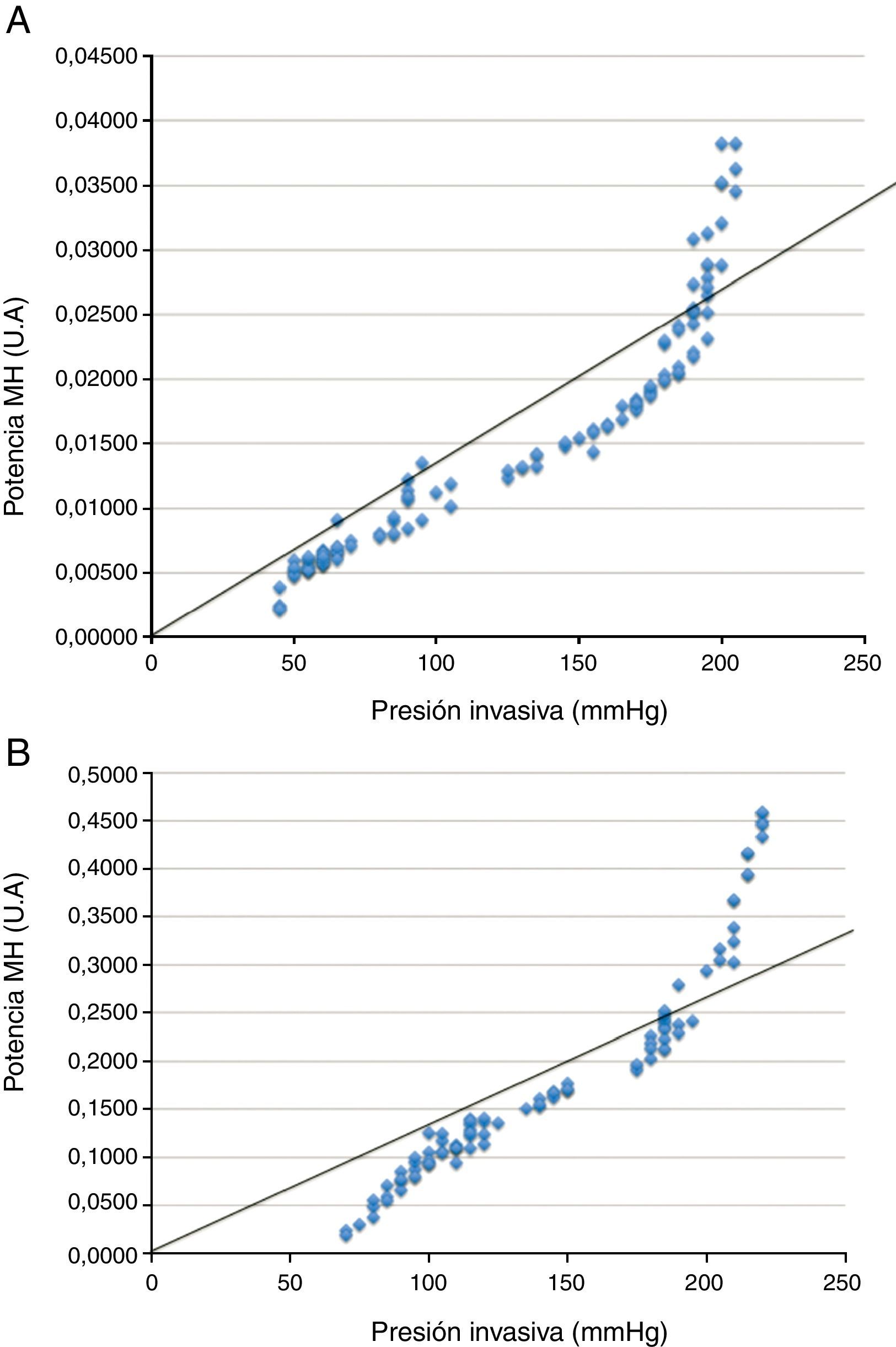
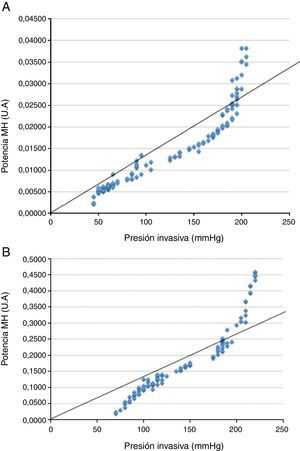
Se obtuvo un índice de correlación de Pearson de 0,941 (p<0,001) entre la presión invasiva del fluido y la potencia MH (fig. 2). No se objetivó una correlación significativa con el resto de variables dependientes.
Medición de la presión del fluido en arteria bovinaLa presión mínima registrada fue de 70mmHg y la máxima de 220mmHg, con una presión media de 143mmHg (DE 32,6).
Se registraron las señales emitidas por el microhilo, observándose un aumento de la amplitud de la señal registrada a medida que aumenta la presión invasiva registrada.
Se obtuvo un índice de correlación Pearson de 0,945 (p<0,001) entre la presión invasiva y la potencia MH (fig. 2). En arteria bovina también se objetivó una correlación significativa entre la presión invasiva y la potencia BIAS (índice de Pearson 0,633; p<0,001).
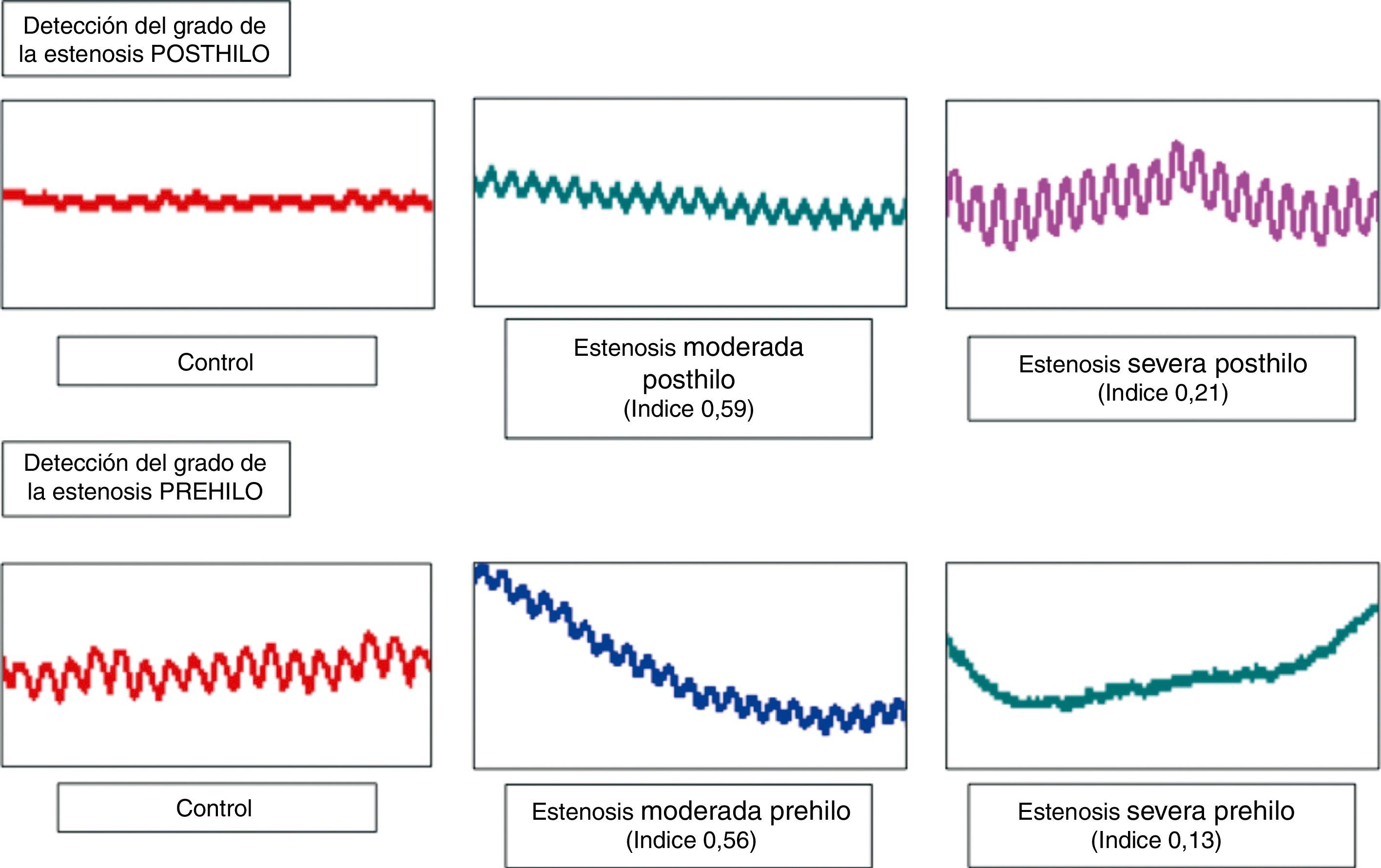
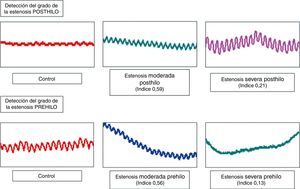
Localización y cuantificación del grado de estenosis en arteria bovinaLa presión media del grupo control fue de 56mmHg (DE 0,1). Posteriormente se realizaron 128 mediciones y se registraron las ondas emitidas por el MH. Se puede apreciar que las estenosis situadas previas al MH amortiguan su señal, mientras que aquellas situadas posteriores al MH producen un aumento de la amplitud del mismo. Además, este cambio es más acentuado cuanto mayor es el grado de la estenosis (fig. 3).
Análisis de FourierSe observó una disminución de la potencia MH en los casos en los que existe una estenosis previa al sensor. Esta disminución es más acusada cuanto mayor es el grado de la estenosis. De igual forma, las estenosis posthilo provocan un aumento de la potencia MH que también es mayor cuanto mayor es el grado de la estenosis.
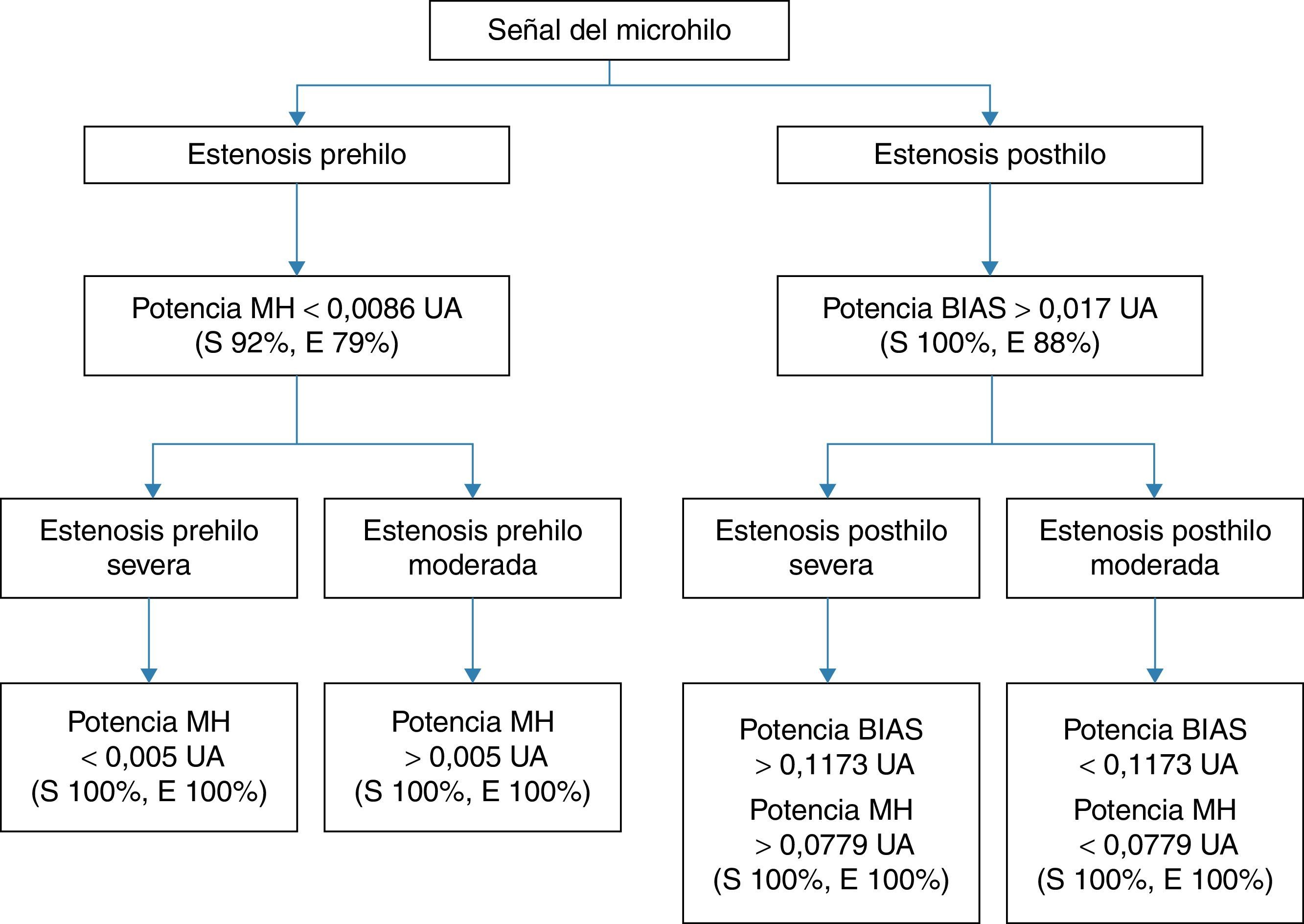
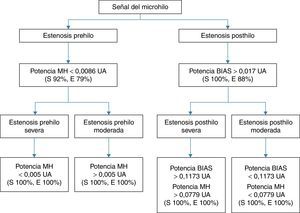
Análisis estadísticoAl analizar las estenosis prehilo (moderadas y severas) y comparar las señales emitidas por el sensor frente al grupo control, la potencia MH obtuvo una curva COR con una muy buena capacidad discriminatoria diagnóstica (AUC 0,93; IC 95%: 0,88-0,98), con una sensibilidad del 92% y especificidad del 79% para el punto de corte de 0,0086 unidades arbitrarias (UA). Para diferenciar los grados de estenosis proximales al MH, se compararon los grupos de estenosis severa frente a moderada, obteniendo una sensibilidad y especificidad del 100% en el punto de corte de potencia MH 0,005UA.
Por otro lado, al estudiar las estenosis posthilo (moderadas y severas) y comparar las señales del microhilo registradas frente al grupo control, la potencia BIAS obtuvo una excelente capacidad discriminatoria (AUC 99; IC 95%: 0,97-1), con una sensibilidad del 100% y una especificidad del 88% en el punto de corte de 0,017UA. Para diferenciar las estenosis posthilo moderadas frente a las severas, un punto de corte de 0,1173UA de potencia BIAS así como una potencia MH de 0,0779UA obtuvieron una sensibilidad y especificidad del 100%.
Por lo tanto, dados los puntos de corte obtenidos en las curvas COR realizadas, podemos seguir el algoritmo descrito en la figura 4, para clasificar una estenosis según los datos obtenidos mediante el microhilo magnetoelástico.
Localización y cuantificación del grado de estenosis en una anastomosis latero-terminal con PTFELa presión media del grupo control fue 155mmHg (DE 0,1). No existieron diferencias significativas ni en la presión media, ni en el grado de las estenosis producidas en los distintos grupos, cuantificado según el índice de presión.
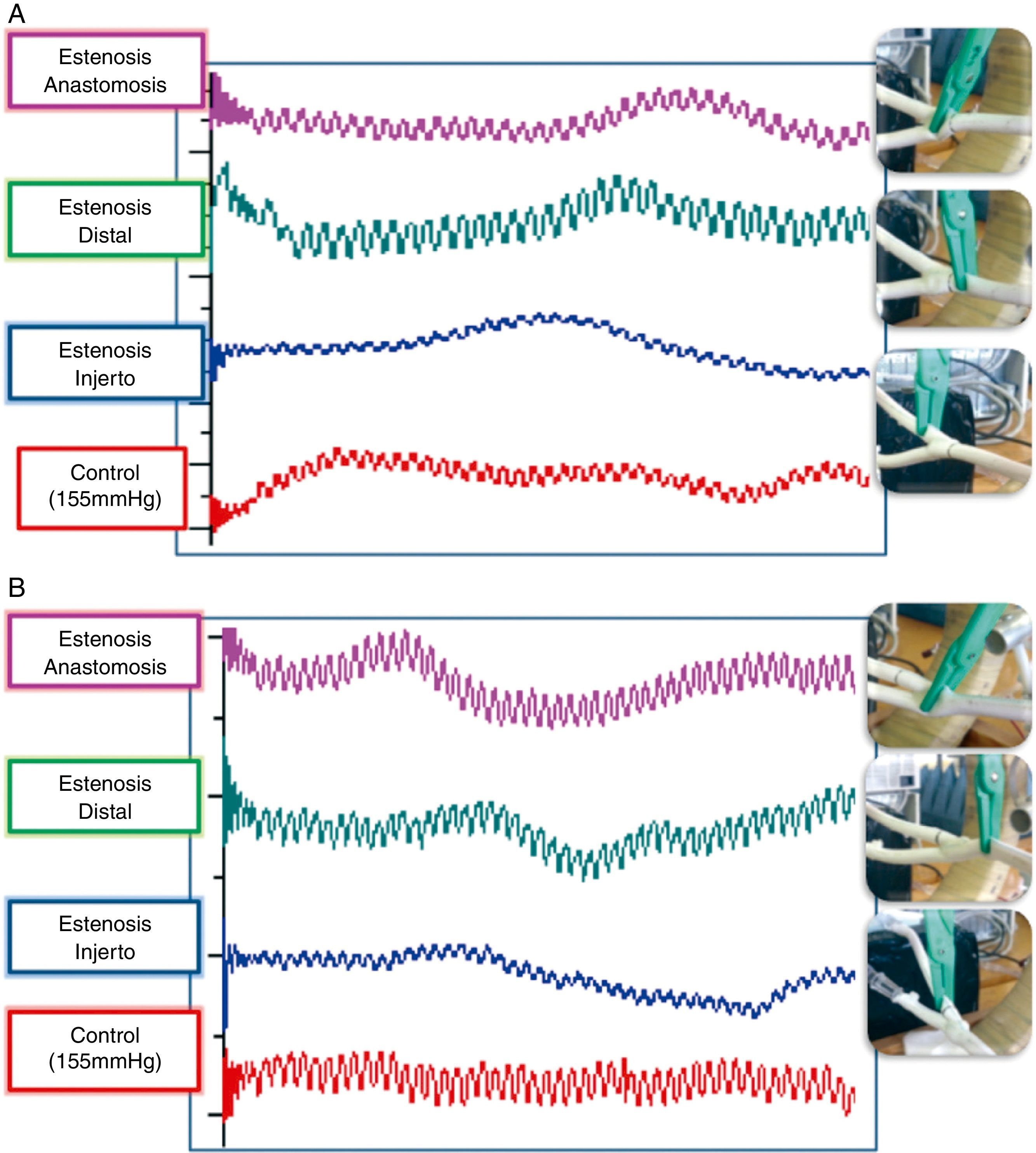
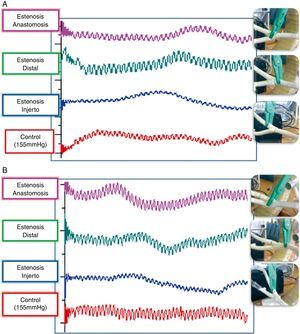
Se registraron las ondas correspondientes a los distintos grupos, observando grandes similitudes morfológicas en las ondas correspondientes al mismo tipo de estenosis entre ambos grupos (fig. 5).
En el caso del grupo A, tal y como se observó en los registros previos, las estenosis proximales al sensor producen una disminución de la amplitud de la onda emitida, mientras que las estenosis distales al mismo producen un aumento de la amplitud de la señal.
Sin embargo, en el caso del grupo B, al variar la posición del MH respecto a la anastomosis, se puede observar como las estenosis en la anastomosis provocan una disminución de la amplitud de la señal al igual que las estenosis en el injerto.
Al comparar las señales, se puede observar como las ondas registradas en las estenosis en el injerto son morfológicamente similares en ambos grupos. En el caso de las estenosis distales, se produce un aumento de la amplitud de las señales, más acentuado en el caso del grupo B. Sin embargo, en el caso de las estenosis anastomóticas, las señales entre ambos grupos son morfológicamente distintas. En el caso del grupo A, la estenosis es distal al MH por lo que produce un aumento de la amplitud respecto al grupo B, en el cual la estenosis es previa al sensor.
Análisis de FourierTanto la potencia MH como la potencia BIAS aumentan en las estenosis producidas distales al sensor en ambos grupos. Por otro lado, dichas potencias disminuyen en el caso de las estenosis producidas proximales al sensor. No obstante, es importante destacar que en el caso de las estenosis distales, la potencia BIAS aumenta de forma más notable en el grupo B (sensor distal a la anastomosis). De igual manera, la potencia MH es menor en las estenosis del injerto en el grupo B respecto al grupo A.
Análisis estadísticoEn términos generales, la posición del MH inmediatamente distal a la anastomosis (grupo B) fue capaz de discriminar mejor los distintos tipos de estenosis frente al grupo control así como entre ellas.
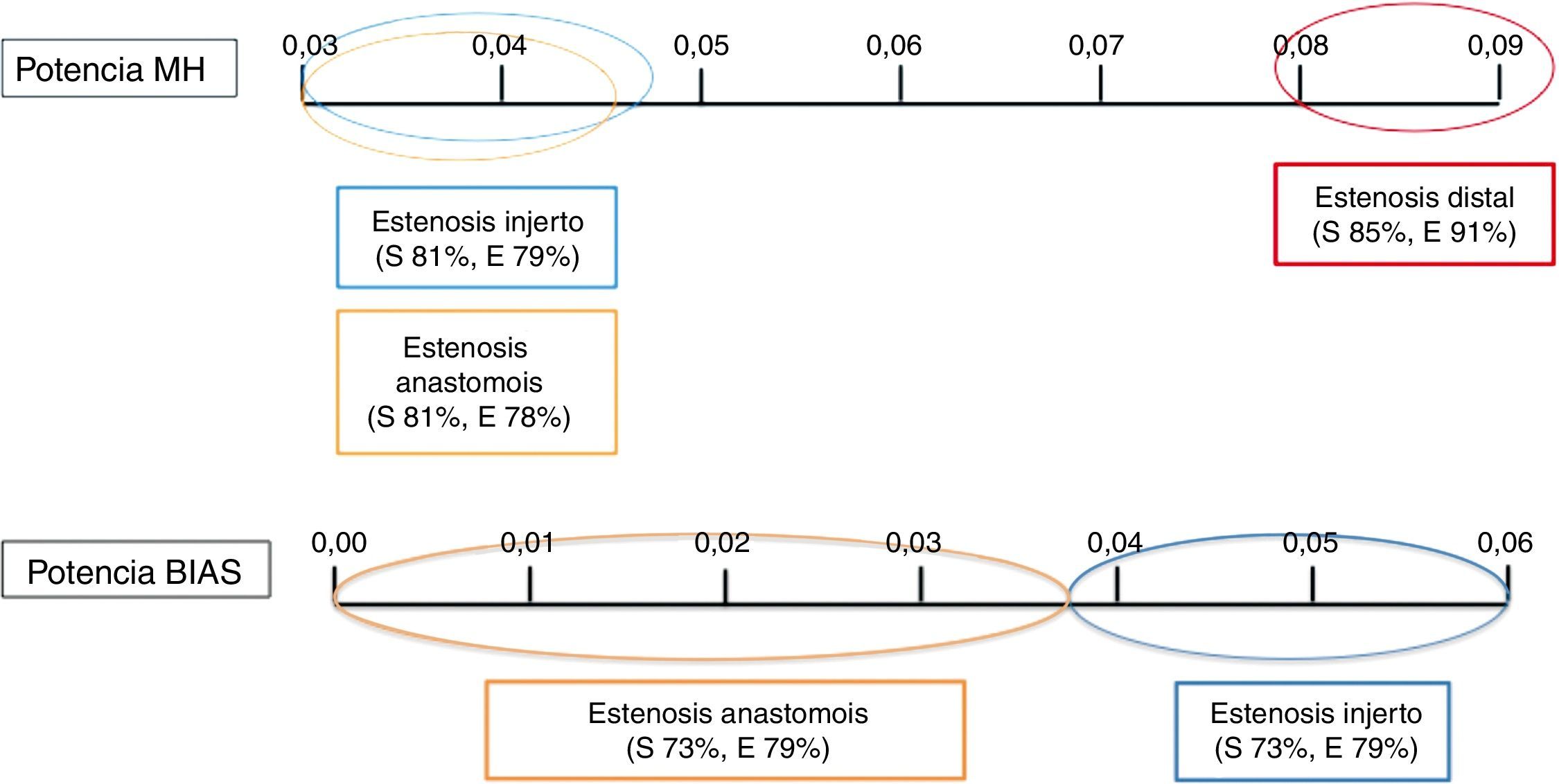
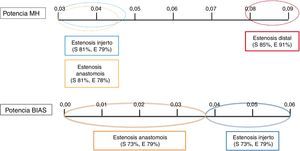
Una potencia MH mayor de 0,0794UA fue capaz de diagnosticar las estenosis distales frente al grupo control con una sensibilidad del 85% y una especificidad del 91% (AUC 0,88; IC 95%: 0,79-0,98).
Para diferenciar las estenosis del injerto frente al grupo control, la potencia BIAS obtuvo una excelente capacidad discriminatoria diagnóstica (AUC 0,98; IC 95%: 0,97-1). El punto de corte de 0,0436UA obtuvo una sensibilidad y especificidad del 97 y 85% respectivamente. Además, la potencia MH obtuvo una curva COR con un AUC: 0,86 (IC 95%: 0,76-0,96). Un valor menor de 0,0473UA fue capaz de clasificar las estenosis del injerto con una sensibilidad del 81% y una especificidad del 79%.
Por último, la potencia BIAS obtuvo una muy buena capacidad discriminatoria (AUC 0,93; IC 95%: 0,86-0,99). Un valor menor de 0,0531UA obtuvo una sensibilidad del 94% y una especificidad del 85% para clasificar las estenosis de la anastomosis frente al grupo control. La potencia MH obtuvo una curva COR con un AUC: 0,82 (IC 95%: 0,71-0,94). Un valor menor de 0,0452UA obtuvo una sensibilidad del 81% y una especificidad del 78%.
Por lo que, si analizamos tan solo la potencia MH en una anastomosis latero-terminal, se pueden clasificar con una elevada fiabilidad las estenosis distales, mientras que las señales emitidas en el caso de los otros 2 tipos de estenosis serían similares, tal y como muestra la figura 6.
Al comparar las señales registradas en las estenosis de la anastomosis frente a las estenosis del injerto, se objetivó que la potencia BIAS obtuvo una curva COR con un AUC: 0,85 (IC 95%: 0,77-0,92). El punto de corte de 0,0378UA clasificaba dichas estenosis con una sensibilidad del 73% y una especificidad del 79%. Por lo tanto, en aquellos casos en los cuales la potencia MH no clasifique el tipo de estenosis (potencia MH menor de 0,0473UA), será la potencia BIAS la cual diferencie si se trata de una estenosis de la anastomosis o del injerto, tal y como muestra la figura 6.
En el grupo A, se objetivó que el sensor fue capaz de clasificar las estenosis del injerto así como las estenosis de la anastomosis frente al grupo control y respecto al resto de estenosis con una elevada capacidad discriminativa diagnóstica. Sin embargo, la sensibilidad del microhilo disminuyó al clasificar las estenosis distales a la anastomosis frente al resto de estenosis del grupo A (AUC 0,67; IC 95%: 0,57-0,78), no siendo capaz de diferenciar las estenosis distales a la anastomosis respecto al grupo control.
DiscusiónLos continuos avances en ciencia y tecnología, así como el progreso social y sanitario experimentado en las últimas décadas han aumentado la esperanza de vida en la población mundial, provocando importantes consecuencias sociales y económicas. Este hecho, unido al aumento de la incidencia y prevalencia de enfermedades crónicas, como las enfermedades cardiovasculares10, ha provocado un cambio en la organización sanitaria en los últimos años, ya que el 5% de los pacientes son responsables del 50% del gasto sanitario11. Así, la creciente carga asistencial y económica producida por estas enfermedades constituye un poderoso incentivo para desarrollar nuevas estrategias para el cuidado de estos pacientes.
El desarrollo de sensores aplicados a la medicina ha evolucionado de forma espectacular en los últimos años. Esto se ve reflejado en los más de 4.200 artículos publicados en 2013 acerca de nuevos biosensores y sus aplicaciones. El primer artículo fue publicado en 1958 y posteriormente tan solo se publicaron 19 artículos en los años sesenta, en los que los sensores consistían en sencillos dispositivos dieléctricos capaces de detectar cambios en la presión del vapor de agua12.
En 2007, nuestro grupo desarrolló un sensor magnético con una elevada sensibilidad para la detección precoz de la degeneración de las válvulas biológicas cardiacas que se basó en detectar de forma inalámbrica los movimientos de unos fragmentos de MH unidos a los velos de una válvula biológica cardiaca13.
En 2011, un grupo japonés desarrolló con éxito un sensor de actividad eléctrica miocárdica utilizando un MH como elemento sensor. Se basaba en la capacidad de detectar el campo magnético producido por la actividad eléctrica del miocardio durante el ciclo cardiaco de una forma totalmente inalámbrica y con una mayor sensibilidad que el electrocardiograma para la detección de arritmias cardiacas e isquemia miocárdica14.
Marín et al. desarrollaron recientemente un nuevo microhilo amorfo, con un elevado factor de acoplo magnetoelástico, con el que obtuvieron unos resultados excelentes sin necesidad de un campo magnético externo, lo que facilita la integración de este material en biosensores de pequeño tamaño y uso más sencillo en aplicaciones biomédicas6.
Por lo tanto, podemos apreciar como el campo de los sensores magnéticos se encuentra en continua evolución, habiendo demostrado numerosas ventajas en aplicaciones biomédicas y aún con un gran potencial por descubrir, como muestran las investigaciones más recientes.
En la presente investigación, se ha desarrollado por primera vez un sensor inalámbrico para el seguimiento de procedimientos en enfermedad vascular con el cual se han obtenido unos excelentes resultados en términos de correlación entre la potencia MH y las presiones registradas. Con base en estos resultados, la potencia BIAS parece modificarse a partir de un umbral de variación de la potencia MH. Es decir, para variaciones pequeñas de la potencia MH, la potencia BIAS no se ve modificada, mientras que para variaciones mayores de la potencia MH, la potencia BIAS comienza a variar de una forma proporcional.
Por lo tanto, la variación de la potencia BIAS únicamente en arteria bovina puede ser debida a la menor rigidez de esta respecto al PTFE y a su mayor complianza. Según Tiwari et al., la complianza de la arteria sana (0,059%/mmHg) es mayor que la del PTFE (0,016%/mmHg), por lo que es capaz de transmitir mejor un flujo pulsátil. No obstante, la complianza de la arteria disminuye a medida que avanza la edad y progresa la enfermedad arterioesclerótica15, por lo que en el futuro, y para asegurar una monitorización duradera de los procedimientos vasculares, creemos que es más efectiva la posición del anillo sensor en PTFE. Además, la localización en material protésico permitiría en el futuro incorporar el MW al tejido de fabricación, por lo que aumentaría la superficie de contacto entre el sensor y el injerto aumentando probablemente la sensibilidad. No obstante, dichos hallazgos deberán ser confirmados en estudios posteriores en animales experimentales.
El MH ha sido capaz de localizar y cuantificar las estenosis provocadas en arteria bovina y en una anastomosis latero-terminal de PTFE con un elevado poder estadístico. Se ha comprobado que la posición de la estenosis respecto al sensor provoca una modificación en la morfología de la señal registrada, que es más evidente cuanto mayor es el grado de la estenosis. Además, es importante destacar que con base en los resultados expuestos, creemos que la distancia entre la estenosis y el sensor afecta a la señal emitida por el sensor, lo cual aumentaría la aplicabilidad y versatilidad del sensor. Esto será motivo de estudio en futuras investigaciones.
El sensor ha clasificado correctamente un porcentaje significativo de estenosis de cualquier grado tanto en posición previa al sensor como distal a él y ha sido capaz de diagnosticar correctamente el 100% de las estenosis severas en arteria bovina. Estos resultados han sido obtenidos en condiciones ideales de laboratorio, por lo que no son extrapolables a la práctica clínica y deberán ser confirmados en futuros estudios.
Existen numerosos artículos que muestran los resultados de distintos programas de telemonitorización. Un artículo de revisión en el que se incluyeron 65 estudios realizados en Europa y Estados Unidos que analizaban los programas de telemonitorización de distintas enfermedades concluyó que la monitorización domiciliaria de las enfermedades crónicas ofrecía datos precisos y fiables con mínimos problemas técnicos. Además, influía en la actitud del paciente, aumentando su compromiso en el control de la enfermedad, lo que potencialmente mejoraría sus condiciones médicas16.
Por lo tanto, aunque el diseño, desarrollo e implementación de los sistemas WSN/WBAN representa una tarea difícil con varias cuestiones de una elevada dificultad técnica, los beneficios de su utilización para la prevención, el diagnóstico precoz y la gestión de las enfermedades son múltiples y ampliamente documentados16-21.
Actualmente, existen protocolos de seguimiento para los distintos procedimientos en cirugía vascular con el fin de identificar aquellos injertos malfuncionantes que precisen ser reintervenidos y de ese modo mantener su permeabilidad. Existe, sin embargo, una falta de consenso en cuanto a las pruebas que deben realizarse, en la frecuencia de las evaluaciones en el postoperatorio, así como en la repercusión costo-efectiva de las distintas estrategias existentes.
Actualmente, el eco-Doppler es la prueba más utilizada para el seguimiento de la cirugía de revascularización de los miembros inferiores. Sin embargo, al tratarse de una prueba explorador-dependiente, cuenta con varias limitaciones, como es el caso de las arterias calcificadas o los injertos profundos. A pesar de la elevada sensibilidad y especificidad del eco-Doppler en el seguimiento de los injertos venosos infrainguinales, existe información contradictoria en cuanto al beneficio en términos de coste-efectividad y de salvación de la extremidad22-28. Además, el seguimiento mediante eco-Doppler no ha demostrado aumentar la permeabilidad de los injertos protésicos29,30 ni de las técnicas endovasculares31,32, por lo que en función de los resultados obtenidos en este estudio y de la eficiencia demostrada de los nuevos métodos inalámbricos de asistencia clínica33, la creación de un nuevo protocolo de seguimiento de los procedimientos en cirugía vascular basado en la tecnología WBAN podría ser de interés en el futuro.
Por lo tanto, el desarrollo de nuevos métodos de seguimiento inalámbricos ofrece numerosas ventajas. En primer lugar, permite evaluar la presión en un punto exacto con una elevada sensibilidad y especificidad. Además, elimina el factor explorador-dependiente, es decir, al tratarse de una prueba inalámbrica y no invasiva se puede realizar de forma ambulatoria sin necesidad de personal especializado e incluso podría realizarse desde el domicilio del paciente, lo cual podría modificar la asistencia postoperatoria a los pacientes intervenidos mediante reconstrucciones vasculares en el futuro.
ConclusionesEl microhilo magnetoelástico ha demostrado una excelente correlación estadística entre la presión de un fluido y la potencia de la señal emitida por el dispositivo, tanto en PTFE como en arteria bovina. Además, es capaz de detectar, localizar y cuantificar el grado de estenosis en arteria bovina, así como en una anastomosis latero-terminal, con una elevada potencia estadística.
Por primera vez se ha desarrollado un sensor inalámbrico in vitro para el seguimiento postoperatorio de los procedimientos en cirugía vascular. No obstante, los resultados obtenidos deberán ser validados en futuras investigaciones en modelos animales.
El desarrollo tecnológico obtenido permite la posibilidad de desarrollar nuevas formas de seguimiento mediante telemetría de los procedimientos en cirugía vascular con numerosas posibles aplicaciones en nuestra especialidad en el futuro.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesNo existen conflictos de interés.
AgradecimientosQuisiera agradecer el enorme trabajo realizado por el Instituto de Magnetismo Aplicado Salvador Velayos.